Células Dendríticas Linfoides o Plasmocitoides (pCDs)
La población de tipo linfoide presente en el
timo, Los progenitores de las CD linfoides o plasmocitoides (pCDs), a
diferencia de las CD mieloides, entran al timo para alojarse y desarrollarse en
la médula tímica, en la unión corticomedular, o viajan directamente, hacia los
órganos linfoides secundarios. Se
desarrollan en CD bajo la influencia de una combinación de las siguientes
citocinas: TNF, IL-1, IL-3, IL-7, factor estimulador de colonia (SCF), ligando
de Flt3 (Flt3L) y ligando de CD40 CD40L.
En contraste, las CD de origen linfoide se localizan en el timo o en las áreas ricas de linfocitos T de los órganos linfoides secundarios y juegan un papel crucial en la inducción de tolerancia central, participando en la selección negativa, tímica, de los linfocitos T autorreactivos.
En los órganos linfoides secundarios reciben el nombre de CD interdigitantes (CDI) y están envueltas en la inducción o mantenimiento de la tolerancia extratímica (periférica) contra antígenos propios o extraños.
En contraste, las CD de origen linfoide se localizan en el timo o en las áreas ricas de linfocitos T de los órganos linfoides secundarios y juegan un papel crucial en la inducción de tolerancia central, participando en la selección negativa, tímica, de los linfocitos T autorreactivos.
En los órganos linfoides secundarios reciben el nombre de CD interdigitantes (CDI) y están envueltas en la inducción o mantenimiento de la tolerancia extratímica (periférica) contra antígenos propios o extraños.
Nota: Las
CD Linfoides Provienen del mismo origen y desarrollo que las CD mieloides, solo
que las CD Linfoides entran el sangre circulante y migran al timo o a órganos
linfoides secundarios de ahí su nombre, por tanto hablare del mismo proceso y
origen de las CD Linfoides (pCDs), quizás la migración de estas es realizada
mediante celulas endoteliales de los vasos sanguíneos en un proceso conocido
como diapédesis.
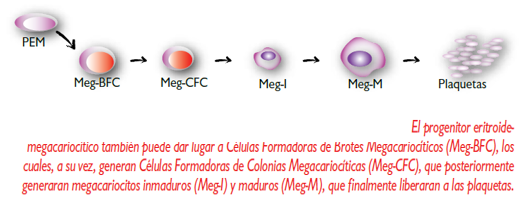
Quien nos interesa para el desarrollo de CD
Linfoides es PGM. Una vez elegido el linaje PGM toda la ruta de
diferenciación es estimulada por factores estimulantes de colonias (CSF),
citocinas e interleucinas (IL).
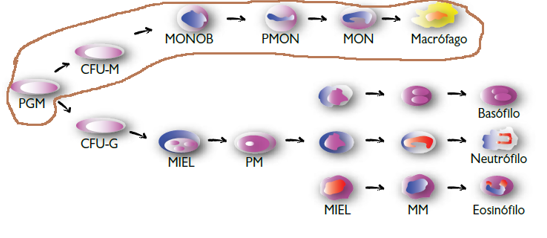
Como tal PGM
genera a su vez a unidades Formadoras de Colonia Granulociticas (CFU-G) y Unidades Formadoras de Colonias
Mielinociticas (CFU-M), para el desarrollo de CD a partir de CFU-M que da lugar
a Monoblastos (MONOB), Promonocito (PMON) y Monocito (MON) entonces el origen
de un Macrófago donde puede
diferenciarse en Célula Dendrítica CD todo esto como ya mencione es propio de la Monopoyesis.
CENTRO DE ESTUDIOS SUPERIORES EN ESTOMATOLOGIA Y SALUD
Equipo 1
•Angel Hernandez Santamaria
•Angel Hernandez Santamaria
•Javier Ramírez Martínez
•Angel Trujillo Arellano
•Kelly Cardoso Ortega
•Daniel Olaf Teyssier Domínguez
Bibliografías
-Tristam G. Parslow Medical Immunology 10th Edition Spanish
-Hematopoyesis (Ruiz Arguelles)
-Gartner's Color Textbook Of Histology 2nd Edition Spanish